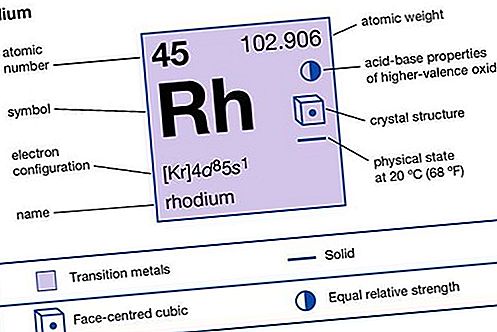
铑(Rh)的化学元素,是元素周期表第5至6组(VIIIb)的铂金属之一,周期表第5和6期,主要用作硬化铂的合金剂。铑是一种宝贵的银白色金属,对光具有高反射率。它在室温下不会被大气腐蚀或失去光泽,并且经常电镀在金属物体上并进行抛光,从而为珠宝首饰和其他装饰性物品提供永久,吸引人的表面。该金属还用于生产光学仪器的反射面。
少量添加到铂中的铑所产生的合金比纯铂更坚硬,并且在高温下失去重量的速度甚至更慢。此类合金用于高温化学环境(包括汽车催化转化器)中的实验室熔炉坩埚,火花塞电极和催化剂。在硝酸的工业生产中,使用了铑-铂合金的纱布催化剂,因为它们可以承受氨燃烧成一氧化氮时的火焰温度。10%铑–90%铂的合金丝与纯铂丝相连,形成了一种出色的热电偶,可用于测量氧化气氛中的高温。通过该热电偶的电动势,在660°至1,063°C(1,220°至1,945°F)范围内定义了国际温度标度。
铑是稀有元素,占天然铂合金的比例高达4.6%。它也存在于铱和的天然合金中:铱胺至少达到11.2%,硅镁石至少达到4.5%。铑与其他铂金属一起自然存在,其分离和精炼构成了该组整体冶金工艺的一部分。铑通常作为从矿石中提取镍和铜的副产品在商业上获得。
天然铑完全由稳定的同位素铑103组成。该元素首先由英国化学家和物理学家威廉·海德·沃拉斯顿(William Hyde Wollaston)从粗铂中分离出来(1803年),后者因其多种化合物的红色而从希腊罗丹(“玫瑰”)中命名。铑具有很高的抗酸侵蚀能力。块状金属不会被热浓硝酸或盐酸甚至王水溶解。在稠合的硫酸氢钾的金属溶解,得到的复合物,水溶性硫酸盐ķ 3的Rh(SO 4)3 ·12H 2 O,在热的浓硫酸,并在浓盐酸含有在125℃-150高氯酸钠° C(257°–302°F)。
铑化学主要集中在+1和+3氧化态上。可以识别到+6的其他一些正氧化态的化合物。铑形成氧化态为+2的四乙酸二铑,Rh 2(O 2 CCH 3)4和含有两个附加配体(例如水,吡啶或三苯基膦)的各种衍生物。氧化态+1的配合物主要包含一氧化碳,烯烃和膦作为配体。通过加热,所有铑化合物都易于还原或分解,从而生成粉末状或海绵状金属。在这些化合物中,三氯化铑中最重要的化合物之一是RhCl 3(其中铑处于+3态)。它为处于各种氧化态的许多其他铑化合物提供了起始原料。在水性乳液中,它可以催化许多有用的有机反应。
元素属性
| 原子数 | 45 |
|---|---|
| 原子重量 | 102.905 |
| 熔点 | 1,966°C(3,571°F) |
| 沸点 | 3,727°C(6,741°F) |
| 比重 | 12.4(20°摄氏度) |
| 氧化态 | + 1,+ 2,+ 3,+ 4,+ 5,+ 6 |
| 电子配置 | [K] 4d 8 5s 1 |