冷冻保存,通过冷冻保存细胞和组织。

伊恩·威尔穆特爵士:教育和冷冻保存研究
威尔穆特(Wilmut)在历史悠久的英国沃里克郡(Warwickshire)的一个小镇考文垂(Coventry)长大,并就读于大学的农业学院
。
低温保存是基于某些小分子进入细胞并防止脱水和细胞内冰晶形成的能力,这可能会导致细胞死亡并在冷冻过程中破坏细胞器。两种常见的防冻剂是二甲基亚砜(DMSO)和甘油。甘油主要用于红细胞的冷冻保护,而DMSO用于保护大多数其他细胞和组织。一种称为海藻糖的糖(存在于能够抵抗极端脱水的生物中)被用于冷冻干燥的冷冻保存方法。海藻糖可稳定细胞膜,对精子,干细胞和血细胞的保存特别有用。
大多数细胞冷冻保存系统都使用可控速率的冰箱。该冷冻系统将液氮输送到放置细胞悬液的密闭室中。仔细监测冷冻速度有助于防止细胞快速脱水和形成冰晶。通常,将细胞从室温移至可控速率冰箱中的约-90°C(-130°F)。然后将冷冻的细胞悬浮液转移到保持在极低温度下且具有处于气相或液相的氮气的液氮冷冻机中。基于冷冻干燥的冷冻保存不需要使用液氮冷冻器。
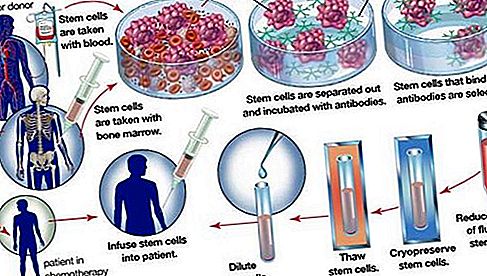
冷冻保存的重要应用是在骨髓和外周血中发现的造血干细胞的冷冻和保存。在自体骨髓抢救中,在用大剂量化学疗法治疗之前,从患者的骨髓中收集造血干细胞。治疗后,将患者的冷冻保存细胞解冻,然后注入体内。由于大剂量化学疗法对骨髓有极高的毒性,因此该程序是必要的。冷冻保存造血干细胞的能力大大增强了某些淋巴瘤和实体瘤恶性肿瘤的治疗效果。对于白血病患者,其血细胞具有癌性,不能用于自体骨髓抢救。结果,这些患者依靠从新生儿的脐带收集的冷冻保存的血液或从供体获得的冷冻保存的造血干细胞。自1990年代后期以来,已经认识到造血干细胞和间充质干细胞(源自胚胎结缔组织)能够分化为骨骼和心肌组织,神经组织和骨骼。如今,人们对组织培养系统中这些细胞的生长以及将这些细胞冷冻保存以用于未来治疗多种疾病(包括神经和肌肉系统疾病以及肝脏和心脏疾病)的强烈兴趣。
冷冻保存还用于冷冻和储存人类胚胎和精子。这对于冷冻通过体外受精(IVF)产生的多余胚胎特别有价值。一对夫妇可以选择将经细胞冷冻的胚胎用于以后的怀孕,或者如果IVF失败而出现新鲜的胚胎。在冷冻胚胎移植的过程中,将胚胎融化并植入女性子宫。冷冻胚胎移植与从此类胚胎出生的儿童中儿童癌症风险的小幅但显着增加有关。
深度低温疗法是人类患者中使用的一种轻度冷冻保存形式,具有重要的应用。诱导深低温的常见用途是用于复杂的心血管外科手术。使用心肺机将患者置于完全的体外循环后,血液通过冷却室。病人的受控降温可能会达到10–14°C(50–57°F)的极低温度。这样的冷却有效地停止了所有脑部活动,并为所有重要器官提供了保护。当达到这种极端冷却时,可以停止心肺机,并且外科医生可以在循环停止期间纠正非常复杂的主动脉和心脏缺陷。在这段时间内,患者体内没有血液循环。手术完成后,血液将在用于冷却的同一热交换器中逐渐加热。逐渐变回正常的体温会恢复正常的大脑和器官功能。然而,这种深刻的低温疗法与冷冻和长期低温保存相去甚远。
如果正确冷冻,细胞可以存活十多年。另外,某些组织,例如甲状旁腺,静脉,心脏瓣膜和主动脉组织,可以成功地冷冻保存。冷冻还用于保存和维持早期人类胚胎,卵子(卵)和精子的长期生存能力。这些组织所用的冷冻程序已经确立,并且在存在冷冻保护剂的情况下,组织可以在-14°C(6.8°F)的温度下长时间保存。
研究表明,在没有冷冻保护剂的情况下冷冻的整个动物在融化后可产生含有完整DNA的活细胞。例如,在-20°C(-4°F)下保存超过15年的整个小鼠的脑细胞核已用于生成胚胎干细胞系。这些细胞随后被用于产生小鼠克隆。