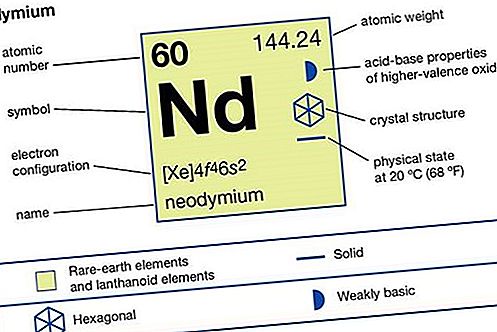
钕(Nd)化学元素,元素周期表中镧系元素的稀土金属。
钕是一种韧性和延展性的银白色金属。它在空气中容易氧化形成Nd 2 O 3氧化物,该氧化物容易剥落,使金属进一步氧化。必须将金属密封保存在塑料盖中或保持在真空或惰性气氛中。它与无机酸逐渐发生反应,氢氟酸(HF)除外,在氢氟酸中形成三氟化物NdF 3保护层。钕是强顺磁性的,在7.5和19.9 K(−265.7和−253.3°C,或−446.2和−423.9°F)时反铁磁有序,并且自发磁矩分别在不同的独立位置(六角形和立方)上发展。
奥地利化学家卡尔·奥尔·冯·韦尔斯巴赫(Carl Auer von Welsbach)于1885年通过反复结晶将钕迪米(稀土氧化物的混合物)制得的硝酸钕迪米铵分离为钕和and部分,从而发现了钕。在稀土中,只有钇,镧和铈比钕更丰富。在地壳的火成岩中,其含量是铅的两倍以上,并且是铜的一半左右。
天然钕是七种不同同位素的混合物。其中五个稳定-钕142(27.13%),钕146(17.19%),钕143(12.18%),钕145(8.30%)和钕148(5.76%)-其中两个是稳定的放射性钕144(23.80%)和钕150(5.64%)。共鉴定了31种钕的放射性同位素(不包括核异构体),其质量范围为124至161,半衰期为0.65秒(钕125)至7.9×10 18年(钕150)。
钕存在于独居石和镁橄榄石矿物中,是核裂变的产物。液-液分离或离子交换技术用于分离和纯化钕。金属本身是通过熔融卤化物的电解或氟化物与钙的金属热还原而制备的。钕存在两种同素异形体(结构形式):在室温下,α相为双密堆积六方晶,a = 3.6582Å,c = 11.7966Å。β相为体心立方,在883°C(1,621°F)时a = 4.13Å。
钕的主要应用是基于Nd 2 Fe 14 B的高强度永磁体,该永磁体用于高性能电动机和发电机,以及计算机硬盘驱动器和风力涡轮机的主轴磁体。这种金属用于电子工业,钢铁制造中,并作为许多铁和非铁合金的一种成分,其中包括混合用于轻火石的金属(钕含量为15%)。金属本身以及与另一种镧系元素的合金已被用作低温低温冷却器应用中的蓄热器,以冷却至4.2 K(-269°C或-452°F)。它的化合物在陶瓷工业中用于釉料,并为玻璃(从粉红色到紫色)提供各种着色。钕稳定钇铝石榴石(YAG)是许多现代激光器的组成部分,钕玻璃用于光纤。钕和ase的混合物吸收有害的钠D光谱线区域的光,因此被用于焊工和吹玻璃者的护目镜玻璃中。
其化合物中的元素,例如氧化物Nd 2 O 3和氢氧化物Nd(OH)3几乎始终处于+3氧化态;Nd 3+离子在水中稳定。仅制备了几种+2态的钕化合物,例如二碘化物NdI 2和二氯化物NdCl 2。Nd 2+离子在水溶液中不稳定。
元素属性
| 原子数 | 60 |
|---|---|
| 原子重量 | 144.24 |
| 熔点 | 1,021°C(1,870°F) |
| 沸点 | 3,074°C(5,565°F) |
| 比重 | 7.008(25°C或77°F) |
| 氧化态 | +2(稀有,不稳定),+ 3 |
| 电子配置 | [Xe] 4f 4 6s 2 |