铀(U),元素周期表中in系元素的放射性化学元素,原子序数92。它是一种重要的核燃料。

in系元素
。
该组织的成员,包括铀(最熟悉),是自然产生的,大多数是人造的。铀和p都被使用了
。
铀约占地壳的百万分之二。一些重要的铀矿物包括沥青闪石(不纯的U 3 O 8),铀矿(UO 2),卡诺石(钒酸铀钾),钙铁矿(磷酸钙铀)和菱锰矿(磷酸铜铀)。作为核燃料来源的这些铀矿和其他可回收铀矿,其能量比所有已知的化石燃料可回收矿床多许多倍。一磅铀可产生140万公斤(300万磅)煤炭的能量。
有关铀矿床以及采矿,精炼和回收技术覆盖范围的其他信息,请参见铀加工。有关铀生产的比较统计数据,请参见表。
铀
| 国家 | 2013年矿山产量(公吨) | 占世界矿山产量的百分比 |
|---|---|---|
| *估计。 | ||
| 资料来源:世界核协会,《世界铀矿开采》(2014年)。 | ||
| 哈萨克斯坦 | 22,574 | 37.9 |
| 加拿大 | 9,332 | 15.6 |
| 澳大利亚 | 6,350 | 10.6 |
| 尼日尔* | 4,528 | 7.6 |
| 纳米比亚 | 4,315 | 7.2 |
| 俄国 | 3,135 | 5.3 |
| 乌兹别克斯坦* | 2,400 | 4.0 |
| 美国 | 1,835 | 3.1 |
| 中国* | 1,450 | 2.4 |
| 马拉维 | 1,132 | 1.9 |
| 乌克兰 | 1,075 | 1.9 |
| 南非 | 540 | 0.9 |
| 印度* | 400 | 0.7 |
| 捷克共和国 | 225 | 0.4 |
| 巴西 | 198 | 0.3 |
| 罗马尼亚* | 80 | 0.1 |
| 巴基斯坦* | 41 | 0.1 |
| 德国 | 27 | 0.0 |
| 世界总数 | 59,637 | 100 |
铀是一种致密,坚硬的金属元素,颜色为银白色。它具有延展性,可延展性,并且能够进行高抛光。在空气中,金属会失去光泽,细碎后会燃烧成火焰。它是相对较差的电导体。尽管是由德国化学家马丁·海因里希·克拉普罗斯(Martin Heinrich Klaproth)于1789年发现的,他后来以最近发现的天王星行星的名字命名,但金属本身首先是由法国化学家Eugène-MelchiorPéligot于(1841)通过还原四氯化铀(UCl 4)来分离的。钾。
俄罗斯化学家德米特里·门捷列耶夫(Dmitry Mendeleyev)在1869年制定了周期系统,将注意力集中在作为最重的化学元素的铀上,直到1940年发现第一个跨铀元素n为止,这个位置一直保持不变。1896年,法国物理学家亨利·贝克勒在铀中发现了铀。放射性现象,1898年由法国物理学家玛丽和皮埃尔·居里(Pierre Curie)首次使用。后来在许多其他元素中发现了此属性。现已知道,铀在其所有同位素中都具有放射性,自然地由铀238(99.27%,45.1亿年的半衰期),铀235(0.72%,713,000,000年的半衰期)和铀234(0.006%,247,000年半衰期)。这些长的半衰期可以通过测量某些含铀岩石中铅的含量(铀的最终衰变产物)来确定地球的年龄。铀238是放射性铀衰变系列的母体,而铀234是放射性铀衰变系列的子体之一。铀235是the系衰变序列的母体。另请参见放线元素。
在德国化学家奥托·哈恩(Otto Hahn)和弗里茨·斯特拉斯曼(Fritz Strassmann)在1938年末发现慢速中子轰击的铀中的核裂变现象之后,铀元素就成为了广泛研究和广泛关注的话题。出生于意大利的美国物理学家恩里科·费米(Enrico Fermi)于1939年初提出,中子可能是裂变产物之一,因此可以作为链反应继续进行裂变。出生于匈牙利的美国物理学家Leo Szilard,美国物理学家Herbert L. Anderson,法国化学家FrédéricJoliot-Curie及其同事(1939年)证实了这一预测。后调查表明,平均2 1 / 2每原子中子裂变过程中被释放。这些发现导致了第一个自我维持的核链反应(1942年12月2日),第一个原子弹试验(1945年7月16日),第一个掉落在战争中的原子弹(1945年8月6日),第一个原子动力潜水艇(1955年)和第一台全尺寸核动力发电机(1957年)。
裂变是由相对较稀少的同位素铀235(唯一天然存在的易裂变材料)中的慢中子发生的,必须将其与大量同位素铀238分开以用于其各种用途。然而,铀238在吸收中子并经历负β衰变之后,被转变为合成元素p,该元素在慢速中子的作用下易裂变。因此,天然铀可用于转炉和增殖反应堆,其中裂变由稀有铀235维持,而and是通过铀238的manufactured变同时制造的。裂变铀233可以从自然界中丰富的非裂变is同位素-232中合成用作核燃料。铀也很重要,它是通过trans变反应从中制备合成铀元素的主要材料。
铀具有很强的正电性,可与水反应。它溶于酸,而不溶于碱。重要的氧化态是+4(如在氧化物UO 2中,四卤化物,如UCl 4和绿色的水离子U 4 +)和+6(如在氧化物UO 3中,六氟化物UF 6和黄色的铀酰中)离子UO 2 2+)。在水溶液中,铀是最稳定的铀酰离子,具有线性结构[O = U = O] 2+。铀也表现出+3和+5态,但各自的离子不稳定。即使在不含溶解氧的水中,红色的U 3+离子也会缓慢氧化。UO 2 +离子的颜色是未知的,因为即使在非常稀的溶液中,UO 2 +也会发生歧化作用(UO 2 +同时被还原为U 4 +并被氧化为UO 2 2+)。
铀化合物已用作陶瓷的着色剂。六氟化铀(UF 6)是在25°C(77°F)下具有异常高的蒸气压(115 torr = 0.15 atm = 15,300 Pa)的固体。UF 6在化学上具有很高的反应活性,但是,尽管UF 6在蒸气状态下具有腐蚀性,但UF 6已被广泛用于将铀235与铀238分离的气体扩散和气体离心方法。
有机金属化合物是一组有趣且重要的化合物,其中存在将金属与有机基团连接的金属-碳键。Uranocene是organouranium化合物U(C 8 H ^ 8)2,其中铀原子被夹相关的两个有机环层之间环辛四烯Ç 8 ħ 8。它于1968年的发现开启了有机金属化学的新领域。
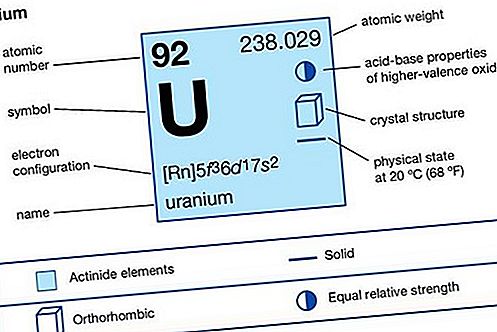
元素属性
| 原子数 | 92 |
|---|---|
| 原子重量 | 238.03 |
| 熔点 | 1,132.3°C(2,070.1°F) |
| 沸点 | 3,818°C(6,904°F) |
| 比重 | 19.05 |
| 氧化态 | + 3,+ 4,+ 5,+ 6 |
| 气态原子态电子构型 | [Rn] 5f 3 6d 1 7s 2 |